نویسنده:
Monica Porter
تاریخ ایجاد:
17 مارس 2021
تاریخ به روزرسانی:
1 جولای 2024

محتوا
غلظت مولی رابطه بین تعداد مولهای ماده محلول و حجم محلول را نشان می دهد. برای محاسبه مولاریت می توانید با مول و حجم ، جرم و حجم یا خال و میلی لیتر (میلی لیتر) شروع کنید. سپس ، با متغیرهای بالا ، فرمول اساسی غلظت مولی را اعمال کنید تا نتیجه صحیح بدست آورید.
مراحل
روش 1 از 4: غلظت مول را از تعداد مول و حجم محاسبه کنید
دانستن فرمول اساسی برای محاسبه غلظت مولی مهم است. غلظت مولی برابر با تعداد مولهای ماده محلول تقسیم بر حجم محلول در لیتر است. از آنجا ، فرمول زیر را داریم: غلظت مولی = تعداد مول محلول / تعداد لیتر محلول
- مثال: غلظت مولی محلول حاوی 0.75 mol NaCl در 4.2 لیتر محلول چقدر است؟

موضوع را تحلیل کنید. برای محاسبه غلظت مولی ، به تعداد مول و حجم محلول در لیتر نیاز دارید. به دلیل موضوع ارائه شده نیازی به محاسبه این دو مقدار نیست.- مثلا:
- تعداد مول = 0.75 مول NaCl
- حجم = 4.2 لیتر
- مثلا:
تعداد خال ها را بر حجم تقسیم کنید. نتیجه تقسیم خال بر حجم تعداد مول در لیتر محلول یا غلظت مولی آن محلول است.
- مثال: غلظت مولی = تعداد مول محلول / تعداد لیتر محلول = 0.75 مول / 4.2 L = 0.17857142

نتایج خود را ثبت کنید. بسته به درخواست معلم یا تکلیف ، بعد از ویرگول را به دو یا سه عدد بچرخانید. هنگام ثبت نتایج ، "غلظت مولی" را با "M" مخفف کنید و نماد شیمیایی املاح را در آن قرار دهید.- مثلا: 0.179 M NaCl
روش 2 از 4: غلظت مول را از جرم و حجم محاسبه کنید
دانستن فرمول اساسی برای محاسبه غلظت مولی ضروری است. غلظت مولی رابطه بین تعداد مولهای ماده محلول و حجم محلول را نشان می دهد. فرمول غلظت مولی به شرح زیر است: غلظت مولی = غلظت املاح / تعداد لیتر محلول
- مثال مسئله: تعداد مول های محلول را در محلول 3.4 گرم KMnO محاسبه کنید4 در 5.2 لیتر آب.

تجزیه و تحلیل موضوع: برای یافتن غلظت مولی ، به تعداد مول و حجم محلول در لیتر نیاز دارید. اگر این مقادیر داده نشده باشد ، اما از حجم و جرم محلول آگاهی دارید ، می توانید قبل از محاسبه غلظت مولر ، تعداد مول های املاح را تعیین کنید.- مثلا:
- وزن = 3.4 گرم KMnO4
- حجم = 5.2 لیتر
- مثلا:
مولکول جرم املاح را محاسبه کنید. برای محاسبه تعداد مولهای املاح از آن جرم یا گرم املاح ، ابتدا باید مولکول جرم ماده حل شده را تعیین کنید. با افزودن اتم جرم هر عنصر در محلول ، می توان مولکول جرم یک ماده حل شده را تعیین کرد. برای یافتن اتم مکعب هر عنصر ، از جدول تناوبی عناصر استفاده کنید.
- مثلا:
- اتم جرم K = 39.1 گرم
- اتم جرم Mn = 54.9 گرم
- اتم جرم O = 16،0 گرم
- کل اتمهای جرم = K + Mn + O + O + O + O = 39.1 + 54.9 + 16 + 16 + 16 + 16 = 158.0 گرم
- مثلا:
گرم را به خال تبدیل کنید. هنگامی که جرم مولی دارید ، باید تعداد گرم املاح موجود در محلول را در ضریب تبدیل معادل 1 مول در جرم مولکول املاح ضرب کنید. نتیجه این ضرب تعداد مولهای محلول است.
- مثال: گرم املاح * (1 / جرم مولار املاح) = 3.4 گرم * (1 مول / 158 گرم) = 0.0215 مول
تعداد مول را به تعداد لیتر تقسیم کنید. اکنون که تعداد خال ها را محاسبه کردید ، اکنون آن عدد را بر حجم محلول در لیتر تقسیم کنید و غلظت مولی آن محلول بدست خواهید آمد.
- مثال: غلظت مولی = تعداد مول محلول / تعداد لیتر محلول = 0.0215 مول / 5.2 L = 0.004134615
نتایج خود را ثبت کنید. شما باید نتایج را مطابق نیاز معلم جمع کنید ، معمولاً دو تا سه عدد بعد از ویرگول. علاوه بر این ، هنگام نوشتن نتیجه ، "غلظت مولی" را به صورت "M" مخفف کنید و نماد شیمیایی املاح را همراه داشته باشید.
- مثلا: 0.004 M KMnO4
روش 3 از 4: غلظت مولار را از تعداد مول و میلی لیتر محلول محاسبه کنید
باید فرمول غلظت مولار را بدانید. برای محاسبه غلظت مولی. شما باید تعداد مول محلول در هر لیتر محلول را محاسبه کنید ، نه میلی لیتر محلول. فرمول کلی برای محاسبه غلظت مولی: غلظت مولی = تعداد مول محلول / تعداد لیتر محلول
- مثال: غلظت مولی محلول حاوی 1.2 مول CaCl را محاسبه کنید2 در 2905 میلی لیتر آب.
موضوع را تحلیل کنید. برای محاسبه غلظت مولی ، به تعداد مول محلول و حجم محلول در لیتر نیاز دارید. اگر حجم محلول در میلی لیتر در مسئله وجود دارد ، قبل از انجام محاسبه ، باید به حجم معادل آن در لیتر تبدیل کنید.
- مثلا:
- تعداد مول = 1.2 مول CaCl2
- حجم = 2905 میلی لیتر
- مثلا:
میلی لیتر را به لیتر تبدیل کنید. برای تبدیل محلول از میلی لیتر به لیتر ، تعداد میلی لیتر را بر 1000 تقسیم کنید ، زیرا هر لیتر برابر 1000 میلی لیتر است. با تغییر رقم اعشاری 3 رقمی که در سمت چپ مانده است ، می توانید میلی لیتر را به لیتر تبدیل کنید.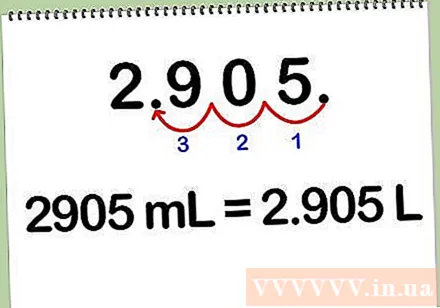
- به عنوان مثال: 2905 میلی لیتر * (1 لیتر / 1000 میلی لیتر) = 2،905 لیتر
تعداد مول را به تعداد لیتر تقسیم کنید. بعد از اینکه تعداد لیتر را داشتید ، می توانید غلظت مولی را با تقسیم تعداد مول بر تعداد لیتر محلول محاسبه کنید.
- مثال: غلظت مولی = تعداد مول محلول / تعداد لیتر محلول = 1.2 مول CaCl2 / 2،905 L = 0.413080895
نتایج خود را ثبت کنید. به یاد داشته باشید که نتیجه را به دو یا سه ویرگول ، یا همانطور که معلم شما درخواست کرده است ، گرد کنید. هنگام ثبت نتیجه ، "غلظت مولی" را به صورت "M" و سپس نماد شیمیایی ماده حل شونده را کوتاه کنید.
- مثلا: 0.413 M CaCl2
روش 4 از 4: تمرین اضافی
غلظت مولی محلول را هنگامی که 5.2 گرم NaCl در 800 میلی لیتر آب حل شد محاسبه کنید. مقادیر داده شده توسط مسئله را تعیین کنید: جرم بر حسب گرم و حجم آن بر حسب میلی لیتر.
- جرم = 5.2 گرم NaCl
- حجم = 800 میلی لیتر آب
با افزودن اتم مکعب عنصر Na و اتم مکعب Cl ، مولکول جرم NaCl را پیدا کنید.
- اتم جرم Na = 22.99 گرم
- اتم جرم Cl = 35.45 گرم
- مولکولهای توده NaCl = 22/99 + 35/45 = 58،44 گرم
جرم املاح را در ضریب تبدیل مولر ضرب کنید. در این مثال ، جرم مولکولی NaCl 58.44 گرم است ، بنابراین ضریب تبدیل "1 مول / 58.44 گرم" است.
- تعداد مول NaCl = 5.2 گرم NaCl * (1 مول / 58.44 گرم) = 0.8898 مول = 0.09 مول
800 میلی لیتر آب را بر 1000 تقسیم کنید ، حجم آب را بر حسب لیتر بدست خواهید آورد.
- همچنین می توانید 800 میلی لیتر را در ضریب تبدیل 1 لیتر در 1000 میلی لیتر از میلی لیتر به لیتر ضرب کنید.
- برای کوتاه کردن روند ضرب مانند بالا ، می توانید 3 رقم اعشار را در سمت چپ برگردانید.
- حجم = 800 میلی لیتر * (1 لیتر / 1000 میلی لیتر) = 800 میلی لیتر / 1000 میلی لیتر = 0.8 لیتر
تعداد مول های املاح را بر حجم محلول در لیتر تقسیم کنید. برای محاسبه غلظت مولی ، باید 0.09 مول محلول (در این مورد NaCl) را بر حجم محلول در لیتر تقسیم کنید.
- غلظت مولی = تعداد مول محلول / تعداد لیتر محلول = 0.09 mol / 0.8 L = 0.1125 mol / L
نتیجه نهایی را ثبت کنید. نتیجه را بعد از کاما به دو یا سه عدد گرد کنید و "غلظت مولار" را با "M" همراه با نماد شیمیایی املاح خلاصه کنید.
- نتیجه: 0.11 M NaCl