نویسنده:
Randy Alexander
تاریخ ایجاد:
2 ماه آوریل 2021
تاریخ به روزرسانی:
1 جولای 2024

محتوا
معادله شیمیایی نمایشی نمادین از یک واکنش شیمیایی است. معرف ها در سمت چپ و محصول در سمت راست نوشته شده اند. قانون حفظ جرم نشان می دهد که هیچ اتمی در واکنش شیمیایی متولد یا از بین نمی رود ، بنابراین تعداد اتم های موجود در واکنش دهنده باید برابر با تعداد اتم های موجود در واکنش باشد. تولید - محصول. به دنبال این آموزش ، می توانید معادلات شیمیایی را به روش های مختلف متعادل کنید.
مراحل
روش 1 از 2: تعادل طبق روش سنتی
معادله داده شده را بنویسید. در این مثال ، شما باید: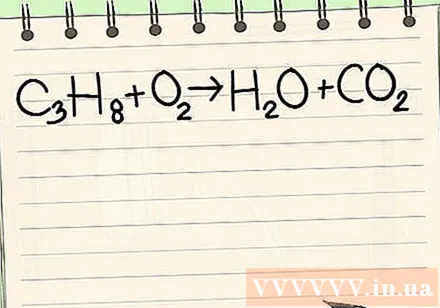
- ج3ح8 + ای2 -> ح2O + CO2
- این واکنش زمانی اتفاق می افتد که پروپان (C3ح8در اکسیژن سوخته و آب و دی اکسید کربن تشکیل می دهد.

تعداد اتم های هر عنصر را که در هر طرف معادله دارید بنویسید. برای یافتن تعداد اتمهای معادله ، شاخص های زیر را در کنار هر اتم مشاهده کنید.- سمت چپ: 3 کربن ، 8 هیدروژن و 2 اکسیژن.
- راست: 1 کربن ، 2 هیدروژن و 3 اکسیژن.
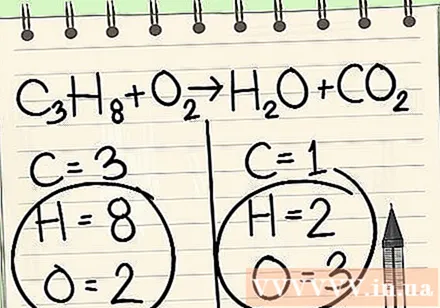
همیشه در پایان هیدروژن و اکسیژن را ترک کنید.
اگر بیش از یک عنصر برای تعادل باقی مانده است: عنصری را انتخاب کنید که فقط در تک مولکول واکنش دهنده و فقط در تک مولکول محصول ظاهر شود. این بدان معنی است که شما ابتدا باید تعادل اتم های کربن را حفظ کنید.
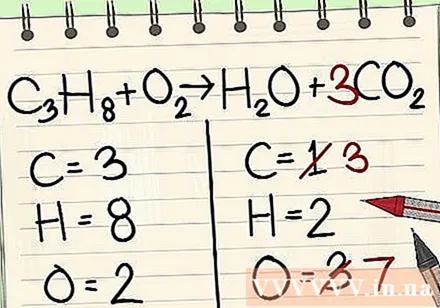
ضریب تک اتمهای کربن را به سمت راست معادله اضافه کنید تا با سه اتم کربن سمت چپ معادله متعادل شود.- ج3ح8 + ای2 -> ح2O + 3CO2
- ضریب 3 در مقابل کربن در سمت راست نشان دهنده وجود 3 اتم کربن است ، دقیقاً مانند شاخص زیر 3 در سمت چپ نشان دهنده 3 اتم کربن است.
- در یک معادله شیمیایی ، می توانید ضریب را تغییر دهید ، اما زیرنویس را تغییر نمی دهید.
بعدی تعادل اتمی هیدروژن است. شما 8 اتم هیدروژن در سمت چپ دارید. از این رو به 8 در سمت راست نیاز خواهید داشت.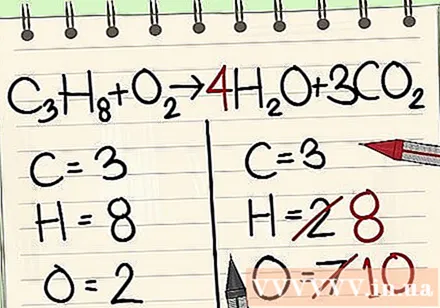
- ج3ح8 + ای2 -> 4 ساعت2O + 3CO2
- در سمت راست ساعت 4 را به عنوان عامل اضافه می کنید زیرا عدد پایین نشان می دهد شما در حال حاضر 2 اتم هیدروژن دارید.
- وقتی ضریب 4 را در شاخص 2 ضرب کنید ، 8 بدست می آورید.
- 6 اتم اکسیژن دیگر از 3CO هستند2(3x2 = 6 اتم اکسیژن + 4 اتم اکسیژن دیگر = 10)
اتمهای اکسیژن را متعادل کنید.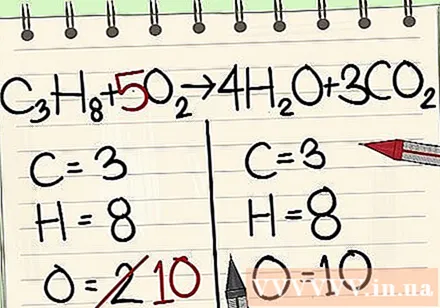
- از آنجا که ضرایب را به مولکولهای سمت راست معادله اضافه کرده اید ، تعداد اتمهای اکسیژن تغییر کرده است. اکنون شما 4 اتم اکسیژن در مولکول آب و 6 اتم اکسیژن در مولکول دی اکسید کربن دارید. در کل ما 10 اتم اکسیژن داریم.
- فاکتور 5 را به مولکول اکسیژن سمت چپ معادله اضافه کنید. اکنون 10 مولکول اکسیژن در هر طرف دارید.
- ج3ح8 + 5 درجه2 -> 4 ساعت2O + 3CO2.

- اتم های کربن ، هیدروژن و اکسیژن در تعادل هستند. معادله شما کامل است.
روش 2 از 2: تعادل مطابق روش جبری
معادلات را با توجه به نمادها و فرمول ها بنویسید. مثال a = 1 و معادله را بر اساس آن فرمول بنویسید.
ارقام را با متغیرهای آنها جایگزین کنید.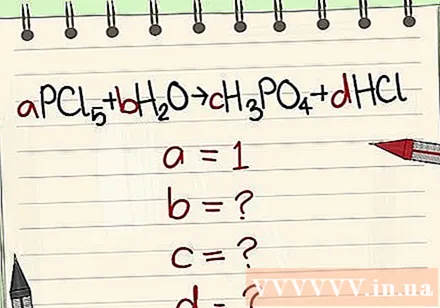
مقدار عناصر موجود در سمت واکنش و همچنین سمت محصول را بررسی کنید.
- مثال: aPCl5 + bH2O = cH3PO4 + dHCl به طوری که a = 1 b = c = d = و عناصر P ، Cl ، H ، O را از هم جدا کنید ، بنابراین a = 1 b = 4 c = 1 d = 5 بدست می آورید .
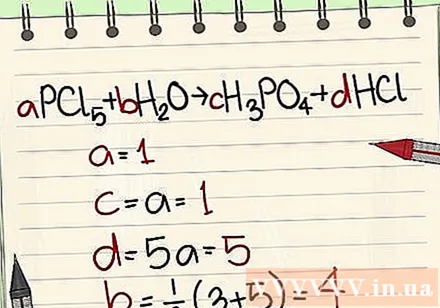
- مثال: aPCl5 + bH2O = cH3PO4 + dHCl به طوری که a = 1 b = c = d = و عناصر P ، Cl ، H ، O را از هم جدا کنید ، بنابراین a = 1 b = 4 c = 1 d = 5 بدست می آورید .
مشاوره
- به یاد داشته باشید که معادله را ساده کنید.
- اگر مشکلی دارید ، می توانید معادله ای را در ابزار تعادل آنلاین تایپ کنید تا تعادل برقرار شود. به یاد داشته باشید هنگام شرکت در امتحان به تعادل آنلاین دسترسی ندارید ، بنابراین به آن وابسته نباشید.
هشدار
- در معادله شیمیایی هرگز از ضریب به عنوان کسر استفاده نکنید - در واکنش شیمیایی نمی توانید مولکول ها یا اتم ها را تقسیم کنید.
- در طی فرآیند تعادل ، می توانید از کسر استفاده کنید ، اما اگر ضرایب هنوز کسری باشند ، معادله متعادل نخواهد بود.
- برای حذف کسرها ، کل معادله (هر دو چپ و راست) را در مخرج کسر ضرب می کنید.