نویسنده:
Bobbie Johnson
تاریخ ایجاد:
10 ماه آوریل 2021
تاریخ به روزرسانی:
1 جولای 2024

محتوا
- مراحل
- قسمت 1 از 2: تجهیزات را آماده کنید
- قسمت 2 از 2: آزمایش را انجام دهید
- نکات
- هشدارها
- چه چیزی نیاز دارید
فرایند تقسیم آب (ح2O) به اجزای تشکیل دهنده آن (هیدروژن و اکسیژن) با استفاده از الکتریسیته الکترولیز گفته می شود. گازهای به دست آمده در نتیجه الکترولیز می توانند به تنهایی مورد استفاده قرار گیرند - به عنوان مثال ، هیدروژن به عنوان یکی از پاک ترین منابع انرژی عمل می کند. اگرچه ممکن است نام این فرایند کمی هوشمندانه به نظر برسد ، اما اگر از تجهیزات ، دانش و تجربه کافی برخوردار باشید ، در واقع آسان تر از آن چیزی است که به نظر می رسد.
مراحل
قسمت 1 از 2: تجهیزات را آماده کنید
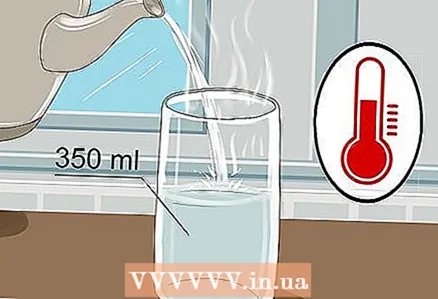 1 یک لیوان 350 میلی لیتری بردارید و آب گرم را داخل آن بریزید. نیازی به پر کردن لیوان تا لبه نیست ، فقط کمی آب کافی است. آب سرد این کار را انجام می دهد ، اگرچه آب گرم برق را بهتر هدایت می کند.
1 یک لیوان 350 میلی لیتری بردارید و آب گرم را داخل آن بریزید. نیازی به پر کردن لیوان تا لبه نیست ، فقط کمی آب کافی است. آب سرد این کار را انجام می دهد ، اگرچه آب گرم برق را بهتر هدایت می کند. - هم آب شیر و هم آب بطری این کار را می کند.
- آب گرم ویسکوزیته کمتری دارد که باعث می شود حرکت یونها راحت تر شود.
 2 1 قاشق غذاخوری (20 گرم) نمک سفره را در آب حل کنید. نمک را در یک لیوان بریزید و آب را هم بزنید تا حل شود. این باعث ایجاد یک محلول شور می شود.
2 1 قاشق غذاخوری (20 گرم) نمک سفره را در آب حل کنید. نمک را در یک لیوان بریزید و آب را هم بزنید تا حل شود. این باعث ایجاد یک محلول شور می شود. - کلرید سدیم (به عنوان مثال نمک سفره) یک الکترولیت است که هدایت الکتریکی آب را افزایش می دهد. آب به خودی خود جریان الکتریسیته را به خوبی هدایت نمی کند.
- پس از افزایش رسانایی الکتریکی آب ، جریان ایجاد شده توسط باتری به راحتی از محلول عبور کرده و مولکول ها را به طور م intoثرتری به هیدروژن و اکسیژن تجزیه می کند.
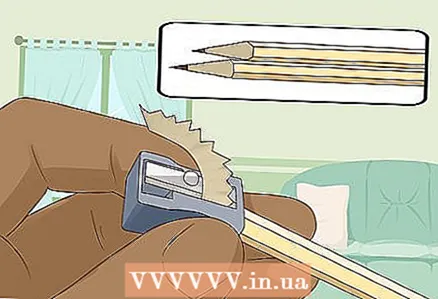 3 دو مداد نرم در دو طرف خود را تیز کنید تا سرب نمایان شود. فراموش نکنید که پاک کن را از مداد خود بردارید. یک میله گرافیت باید در دو انتهای آن بیرون زده باشد.
3 دو مداد نرم در دو طرف خود را تیز کنید تا سرب نمایان شود. فراموش نکنید که پاک کن را از مداد خود بردارید. یک میله گرافیت باید در دو انتهای آن بیرون زده باشد. - میله های گرافیتی به عنوان الکترودهای عایقی عمل می کنند که باتری را به آنها متصل می کنید.
- گرافیت برای این آزمایش مناسب است زیرا در آب حل نمی شود و نمی خورد.
 4 یک ورق مقوا را به اندازه ای ببرید که روی شیشه قرار گیرد. از یک تکه مقوا نسبتاً ضخیم استفاده کنید که بعد از دو سوراخ در آن آویزان نشود. یک قطعه مربع از جعبه کفش یا موارد مشابه برش دهید.
4 یک ورق مقوا را به اندازه ای ببرید که روی شیشه قرار گیرد. از یک تکه مقوا نسبتاً ضخیم استفاده کنید که بعد از دو سوراخ در آن آویزان نشود. یک قطعه مربع از جعبه کفش یا موارد مشابه برش دهید. - مقوا برای نگه داشتن مداد در آب استفاده می شود تا به کناره ها و پایین شیشه برخورد نکند.
- مقوا غیر رسانا است ، بنابراین می توانید با خیال راحت آن را روی لیوان بگذارید.
 5 با استفاده از مداد دو سوراخ روی مقوا ایجاد کنید. مقوا را با مداد سوراخ کنید - در این حالت ، آنها محکم محکم می شوند و نمی لغزند. اطمینان حاصل کنید که گرافیت به کناره ها یا پایین شیشه برخورد نکند ، در غیر این صورت در آزمایش تداخل ایجاد می کند.
5 با استفاده از مداد دو سوراخ روی مقوا ایجاد کنید. مقوا را با مداد سوراخ کنید - در این حالت ، آنها محکم محکم می شوند و نمی لغزند. اطمینان حاصل کنید که گرافیت به کناره ها یا پایین شیشه برخورد نکند ، در غیر این صورت در آزمایش تداخل ایجاد می کند.
قسمت 2 از 2: آزمایش را انجام دهید
 1 یک سیم را با گیره تمساح به هر پایانه باتری وصل کنید. باتری به عنوان منبع جریان الکتریکی عمل می کند و از طریق سیم های گیره و میله های گرافیت ، جریان به آب می رسد.یک سیم را با گیره به مثبت و سیم دیگر را به پایانه منفی باتری وصل کنید.
1 یک سیم را با گیره تمساح به هر پایانه باتری وصل کنید. باتری به عنوان منبع جریان الکتریکی عمل می کند و از طریق سیم های گیره و میله های گرافیت ، جریان به آب می رسد.یک سیم را با گیره به مثبت و سیم دیگر را به پایانه منفی باتری وصل کنید. - از باتری 6 ولت استفاده کنید. اگر باتری ندارید ، می توانید به جای آن از باتری 9 ولت استفاده کنید.
- باتری مناسب را می توان از یک فروشگاه لوازم الکتریکی یا سوپر مارکت تهیه کرد.
 2 انتهای دیگر سیم ها را به مدادها وصل کنید. گیره های سیم فلزی را محکم به میله های گرافیت وصل کنید. برای جلوگیری از سر خوردن گیره ها بر روی میله های گرافیت ، ممکن است لازم باشد چوب بیشتری را از مدادها جدا کنید.
2 انتهای دیگر سیم ها را به مدادها وصل کنید. گیره های سیم فلزی را محکم به میله های گرافیت وصل کنید. برای جلوگیری از سر خوردن گیره ها بر روی میله های گرافیت ، ممکن است لازم باشد چوب بیشتری را از مدادها جدا کنید. - بنابراین ، مدار را می بندید و جریان باتری در آب جریان می یابد.
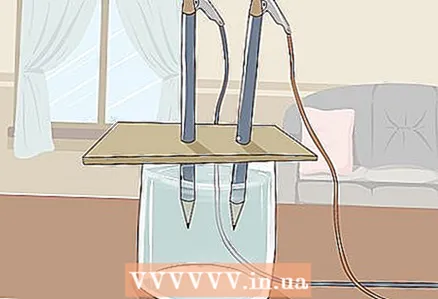 3 مقوا را روی شیشه قرار دهید تا انتهای آزاد مدادها در آب غوطه ور شوند. ورق مقوا باید آنقدر بزرگ باشد که روی شیشه قرار بگیرد. مراقب باشید که محل قرار گیری صحیح مدادها مختل نشود.
3 مقوا را روی شیشه قرار دهید تا انتهای آزاد مدادها در آب غوطه ور شوند. ورق مقوا باید آنقدر بزرگ باشد که روی شیشه قرار بگیرد. مراقب باشید که محل قرار گیری صحیح مدادها مختل نشود. - برای موفقیت آزمایش ، گرافیت نباید به دیوارها و پایین شیشه برخورد کند. این را دوباره بررسی کنید و در صورت لزوم مدادها را تنظیم کنید.
 4 تماشای تقسیم آب به هیدروژن و اکسیژن. حباب های گاز از میله های گرافیت غوطه ور در آب شروع به بلند شدن می کنند. اینها هیدروژن و اکسیژن هستند. هیدروژن در قطب منفی و اکسیژن در قطب مثبت آزاد می شود.
4 تماشای تقسیم آب به هیدروژن و اکسیژن. حباب های گاز از میله های گرافیت غوطه ور در آب شروع به بلند شدن می کنند. اینها هیدروژن و اکسیژن هستند. هیدروژن در قطب منفی و اکسیژن در قطب مثبت آزاد می شود. - به محض اتصال سیم ها به باتری و میله های گرافیت ، یک جریان الکتریکی در آب جریان می یابد.
- حباب های گاز بیشتری روی مدادی که به قطب منفی متصل است تشکیل می شود ، زیرا هر مولکول آب از دو اتم هیدروژن و یک اتم اکسیژن تشکیل شده است.
نکات
- اگر مداد با شافت گرافیت ندارید ، می توانید به جای آن از دو سیم کوچک استفاده کنید. فقط یک سر هر سیم را دور قطب باتری مربوطه بپیچید و سر دیگر را در آب فرو کنید. نتیجه همان مداد خواهد بود.
- سعی کنید از باتری دیگری استفاده کنید. میزان جریان جاری بستگی به ولتاژ باتری دارد که به نوبه خود بر میزان تقسیم مولکول های آب تأثیر می گذارد.
هشدارها
- اگر الکترولیت مانند نمک را به آب اضافه می کنید ، به خاطر داشته باشید که این آزمایش مقدار کمی محصول جانبی مانند کلر تولید می کند. در مقادیر کم ایمن است ، اما می توانید بوی کمی کلر را استشمام کنید.
- این آزمایش را زیر نظر بزرگسالان انجام دهید. این با برق و گازها همراه است و بنابراین می تواند خطرناک باشد ، هر چند بعید است.
چه چیزی نیاز دارید
- دو مداد سخت و نرم
- یک باتری 6 یا 9 ولت
- شیشه با حجم 350 میلی لیتر
- 2 سیم با گیره تمساح
- تیز کننده برای مداد
- نمک